Как решать задачи по физике на силу трения
Движение тела по поверхности другого тела всегда связано с преодолением силы трения. Насколько она замедляет передвижение? В какую сторону направлена? Зависит ли от присутствия между соприкасающимися поверхностями жидкости? Это вопросы, на которые отвечает специальный раздел физики.
Сила трения — что это за показатель?
Соприкосновение двух поверхностей неизменно ведет к появлению силы трения. Ее величина зависит от состояния тел и особенностей их движения:
- между неподвижными телами присутствует трение покоя;
- перекачивающимися — трение качения;
- скользящими — трение скольжения;
- в жидкой среде такой процесс носит название силы сопротивления среды.
Сила, появление которой зависит от соприкосновения двух поверхностей, называется силой трения.
Другими словами, каждое поверхностное движение тем слабее, чем выше трение соприкасающихся сторон. Объясняется это тем, что сила трения всегда направлена против этого движения и распространяется в плоскости, направленной по касательной.
Для понимания данного процесса важно опираться на прямо пропорциональную зависимость силы нормального давления и свойств соприкасающихся поверхностей. Она, в свою очередь, объясняется существованием электромагнитного поля определенной величины.
Естественно, что трение, возникающее внутри механизмов, носит название внутреннего, снаружи — внешнего. Так, если работающий прибор не движется в пространстве, в нем возникают внутренние cилы трения. Если он перемещается относительно других тел, он должен преодолевать внешнюю силу трения.
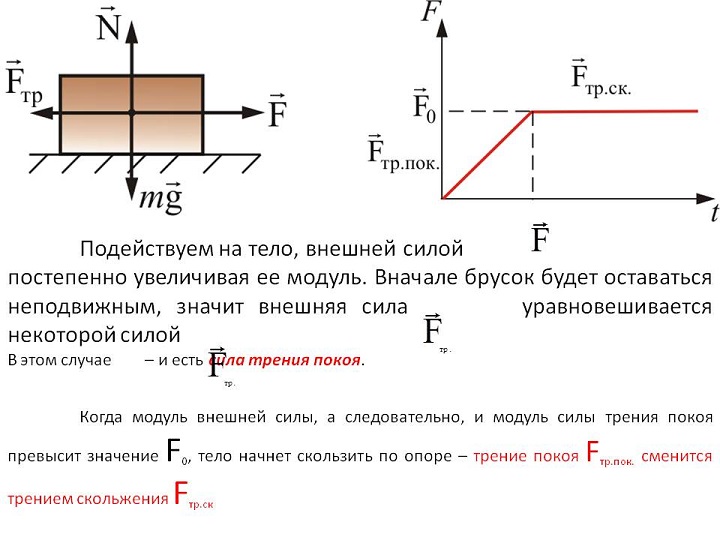
Действие силы трения можно наблюдать на примере:
Тело на горизонтальной поверхности, при отсутствии воздействия на него посторонних сил, лежит неподвижно. Начиная применять некую силу движения Fдв происходит попытка сдвинуть его с места.
Сначала это не удается из-за того, что Fтр превышает величину внешней силы. Увеличивая модель последней, добиваются уравновешивания, а затем — превышение силы движения. В данном случае, сила трения — это сила покоя.
Даже максимальное трение не определяется площадью соприкасающихся поверхностей тел, но зависит от силы \(N\) (нормальное давление) и коэффициента трения покоя \(\mu0\).
\(Fтр\;пок=\mu0N\)
Продолжая увеличивать давление, добиваются того, что тело начинает скользить. Теперь при его движении действует сила трения скольжения, на преодоление которой также должно хватать значения внешней силы.
Если рассматриваемый предмет круглой формы, его движение сопровождается силой трения качения. Коэффициент трения при этом гораздо меньше, хотя особенности процесса идентичны.
Тело, находящееся по поверхности под наклоном, испытывает на себе воздействие дополнительной силы — силы опоры.
Понятие и определение, в каких единицах измеряется
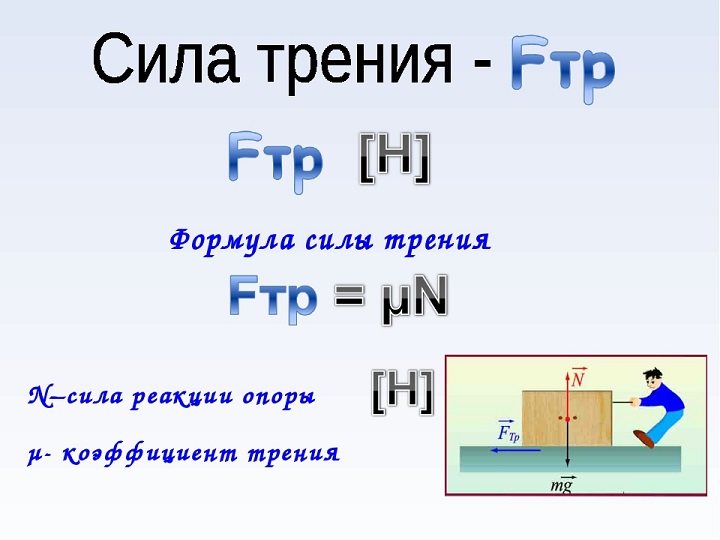
Классической формулой для определения Fтр предмета, лежащего на горизонтальной опоре, является:
\(F=\;k\ast N\)
где \(k\) — коэффициент трения. Это постоянная величина, которая отражается в специальных технических таблицах и зависит от природы вещества.
\(N\) — реакция опоры.
Kоэффициент k может встречаться в виде буквы \mu.
Помимо него, важно правильно определить реакцию опоры. Она высчитывается по формуле: \(N=m\ast g,\) где \(m\) — известная масса тела, g — показатель свободного падения, равный 9,8м/с2.
Предмет, совершающий движение по наклонной поверхности, испытывает на себе воздействие нескольких сил. Поэтому формула для его Fтр принимает вид:
\(Fтр=k\ast m\ast g\ast\cos\alpha\)
В формуле используется гравитационная постоянная g. Ее величина равна 9,8 м/с2.
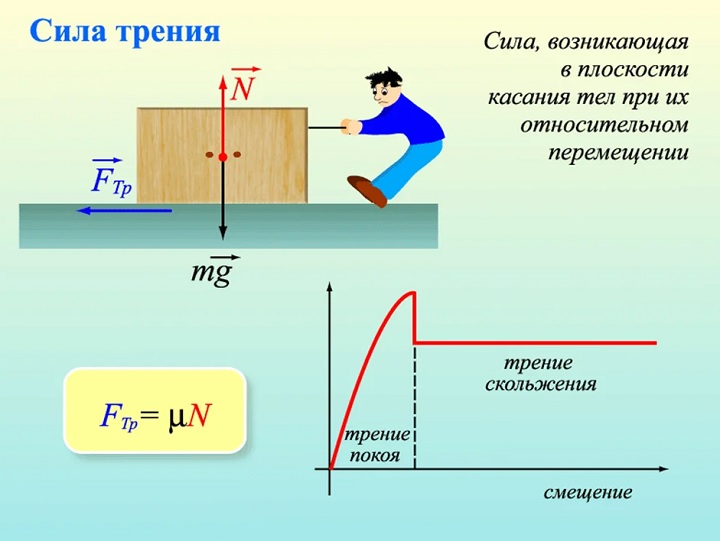
Для измерения силы трения в СИ существует единица Н (Ньютон). В системе CГС она измеряется в динах (дин).
Выразить смысл единицы Ньютон можно формулой:
\(H=кг\ast м/с2\)
Задачи на силу трения, решение типовых примеров
Задания по теме «Сила трения» могут иметь разные направления:
- На определение силы трения.
- На определение коэффициента трения.
- На определение силы трения покоя.
- На определение силы трения скольжения.
- На определение коэффициента трения скольжения.
Пример №1
Масса тела, находящегося на столе, составляет \(5 кг. µ=0,2\). К телу прилагают внешнюю силу, равную \(2,5Н\). Какая сила трения при этом возникает (по модулю)?
Решение: по формуле для максимальной силы трения \(Fмакс\;тр=\mu mg=0,2\ast5\ast10=10Н\)
Внешняя сила по условию задачи меньше, максимальной, поэтому тело находится в покое. Fтр уравновешивает внешнюю силу. Следовательно, она равняется \(2,5Н.\)
Пример №2
Брусок из металла весит 4 кг и лежит на горизонтальной поверхности. Известно, что подвинуть его можно, приложив силу 20 Н, имеющую горизонтальное направление. Если на эту же поверхность положить предмет из пластика с массой 2 кг, необходимая сила значительно изменится. Какой величине она будет равна, если коэффициент трения пластикового предмета в 2 раза меньше металлического.
Решение:
На брусок из металла действует сила согласно формуле \(F1=m1\ast g\ast\;µ1\), на пластиковый — \(F2=m2\ast g\ast\;µ2=µ1/2m2\ast g\).
В начале действия \(F=Fтр\).
Формула, позволяющая решить задачу, имеет следующий вид: \(F2=F1/2\ast m2/m1=1/2\ast20\ast2/4=5Н\).
Пример №3
Санки весят 5 кг. При скольжении по горизонтальной поверхности на полозья действует сила трения 6 Н. Определить коэффициент трения, если ускорение свободного падения в данной ситуации равно 10 м/с2.
Решение: при скольжении полозьев санок по поверхности сила трения скольжения обуславливается силой реакции опоры, а также коэффициентом µ. Формула имеет следующий вид: \(F=\;µN\). С другой стороны, второй закон Ньютона диктует, что \(N=mg\). Отсюда вытекает, что \(µ=F/mg=6H/5кг\ast10м/с2=0,12\).
Пример №4
Тело имеет массу 5 кг. Оно совершает движение в горизонтальной плоскости. При этом сила трения составляет 10 Н. Определить величину силы трения скольжения при условии, что масса уменьшится на 2 кг, а коэффициент останется без изменений.
Решение: сила трения имеет формулу \(F=\;µ\ast N\). Если тело движется горизонтально по опоре, согласно второму закону Ньютона, его \(N\) равняется произведению \(m\ast g\).
Исходя из этого, \(Fтр\) будет пропорциональна массе, умноженной на \(µ\). При неизменном коэффициенте трения уменьшение массы тела в 2 раза приведет к уменьшению силы трения скольжения также в 2 раза. Поэтому:
\(10H/2=5H.\)
Пример №5
Тело, движущееся по ровной горизонтальной плоскости, давит на нее с силой 20 Н. Сила трения при этом составляет 5 Н. Определить величину коэффициента трения скольжения.
Решение: Поскольку \(F=\;µ\ast P,µ=\;Fтр/P\). Подставляя значения, получаем расчет: \(5Н/20Н=0,25.\)
Ответ: \(µ=0,25\).
Получить знания или подготовить контрольную работу по теме «Сила трения» можно быстро и грамотно, если обратиться за помощью на Феникс.Хелп.
Решение задач по статистике в колледже
Проведение любого вида анализа, как оперативного, так и ретроспективного, требует грамотного использования статистических приемов. Они помогают оценить наличие достоверной связи между явлениями, выводят усредненные показатели, которые важны для факторной оценки.
Особенности решения задач по статистике в колледжах и вузах
На современном этапе развития общества применение методов статистической обработки материала позволяет:
- проанализировать те или иные явления, определив характер и выявив закономерности;
- спрогнозировать ситуацию на близкую либо отдаленную перспективу;
- спланировать перечень мероприятий для корректировки выявленной тенденции.
Статистика применяется в экономике, здравоохранении, педагогическом анализе, бизнесе, социальных науках и общественных явлениях.
В учебных программах колледжей и вузов обязательно присутствует курс статистики, целью которого является научить студентов статистической методологии, правилам применения статистических выводов в практической деятельности специалиста.
Статистика является целостной системой, затрагивающей как социально-экономическое, так и отраслевое направление, часто имеет международный характер.
Решение задач по статистике в учебных заведениях среднего и высшего звена опирается на утвержденные алгоритмы, смыслом которых является четкое следование оговоренным этапам.
- Сбор данных. При этом в работу берутся не все показатели. Исключение составляют, например, годы, когда действовали факторы непреодолимой силы (стихийные бедствия, эпидемии и т.п.). Таким образом, формируются выборки показателей, каждая из которых предназначена для определенной статистической обработки.
- Обобщение выбранных данных – преподаватель дает студенту характеристику существующих методов и способов получения показательного результата, выведения закономерностей и подтверждения их графически.
- Анализ. Устанавливаются связи между явлениями или факторами, наблюдается наличие взаимосвязи между количественными и качественными показателями.
- Итог. Определение динамики того или иного процесса, характеристика демографических процессов среди населения либо прочих анализируемых факторов.

Формируя определенную совокупность для статистической обработки, обращают внимание на частоту встречаемости того или иного признака или варианта. Тот из них, который встречается чаще других, статистически обозначает «моду». Благодаря ему формируется обобщающая характеристики величины признака. Обозначается мода Мо. При рассмотрении дискретного ряда (т.е. ряда, образованного числами) мода выделяет то значение, которое встречается чаще остальных.
Существует еще одна характеристика выстроенного динамического ряда. Это медиана. Она находится в середине вариационного ряда, построенного по принципу возрастания или убывания, и делит его на две половины.
Мода и медиана в математике называются распределительными средними. Их основное назначение сводится к формированию общей характеристики выбранного варьирующего признака какой-то величины.
Методы расчета ошибки выборки
Задачи со статистическими методами решений имеют в своей основе генеральную совокупность. Под этим термином понимается суммарное количество предметов наблюдения, которые имеют тот или иной общий признак.
Пример
Населенный пункт можно охарактеризовать численностью населения, количеством имеющихся на территории промышленных предприятий, учреждений образования, здравоохранения и т.д.
Выбрав нужный признак, его характеристики отбираются и объединяются в выборку (выборочную совокупность). Однако необходимо помнить, что для обеспечения полноценного действия полученного в результате анализа вывода, каждая выборка должна быть репрезентативной.
Репрезентативность выборки можно продемонстрировать на следующем примере. Отобрав значения показателей детей, посещающих детские дошкольные учреждения в Москве и получив выводы, его нельзя применить ко всей Московской области либо ко всей стране.
Кроме репрезентативности, каждая выборка может иметь ошибку. Ошибка выборки может возникнуть по причине недостаточного количества ее размера. Другими словами, в изучаемом процессе недостаточный доверительный интервал.
Ошибки можно дифференцировать на:
- статистическую;
- систематическую.
Именно статистическая определяется размером выборки. С увеличением числа наблюдений она уменьшается.
Систематическая ошибка не математического характера. Она зависит от воздействия определенных факторов, которые могут сместить результаты наблюдения в ту или иную нетипичную сторону.
В математике, когда говорят об ошибке выборки, имеют ввиду статистическую.
Рассмотрим расчет ошибки выборки для обобщения результатов опроса респондентов. Обычно такие социальные исследования носят выборочный характер, т.е. опрашиваются не 100% людей, а некоторая часть. Именно поэтому нельзя быть уверенным в полученном результате на 100%.
Определить ошибку выборки можно по следующим формулам:
1. \(\Delta=Ζ\surd(p\times g\div n)\)
Она применяется для тех ситуаций, когда размер выборки намного меньше чем сама генеральная совокупность.
2. Для случаев с незначительной разницей между объемом выборки и генеральной совокупностью рекомендуется формула:
\(\Delta=Ζ\surd(p\times q\div n\times((N-n)\div(N-1))\)
Условные обозначения:
Δ - предельная ошибка
Ζ - коэффициент доверительного уровня
N - величина генеральной совокупности
n - объем выборки
p - часть опрошенных, у которых есть исследуемый признак
q = 1−p - те опрошенные, которые не имеют исследуемого признака
Статистическая сводка и группировка
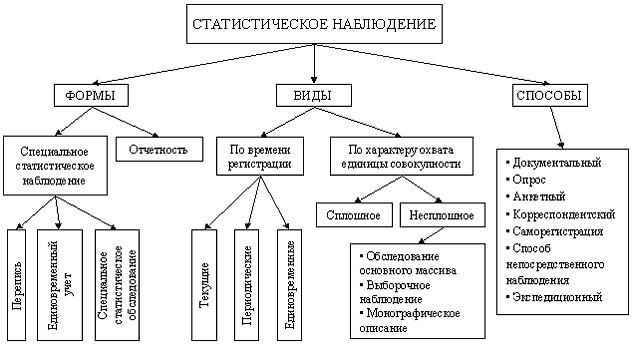
После этапа статистического наблюдения следует составление статистической сводки. Его цель – систематизация имеющейся информации, составление общей характеристики для рассматриваемой совокупности.
Алгоритм операций, начиная с первичной обработки имеющихся данных, имеющий своей целью выделение типичных свойств описывающих изучаемое явление, называется статистической сводкой. Он включает подсчет групповых и обобщенных результатов, группировку сведений и составление табличной формы анализа.
Дифференцируют простую и сложную сводку. При простой в качестве результата анализа имеют общие итоги. При сложной – итоги в виде анализов по группам, возможно, объединенных в таблицы.
Основными этапами составления сводки являются:
- отбор признака, по которому будет проводиться группировка;
- обозначение последовательности, которая ляжет в основу формирования каждой группы;
- определение системы показателей, которые будут статистически характеризовать каждую группу и совокупность;
- составление таблиц с целью наглядной демонстрации полученных результатов.
Метод статистической обработки путем группировки применяется, когда вся исследуемая генеральная совокупность может быть разделена на группы по выбранному признаку. Этот признак называется группировочным.
Таким образом, группировка – это один из способов выделения в совокупности данных, характеризующих выбранный признак. Такое изучение имеет своей целью изучить структуру совокупности, выявить возможную взаимосвязь между изучаемыми признаками. Например, применяя группировку, легко выделить в большой организации участки с высоким выполнением запланированных показателей.
В экономической отрасли группировка применяется если нужно проанализировать трудовые ресурсы, наличие средств труда, материальные ресурсы и т.п.
Сегодня выделяют следующие виды группировок:
- простая;
- сложная;
- типологическая;
- структурная;
- аналитическая и др.
При структурной группировке могут исследоваться состав и структура имеющегося статистического материала. При аналитической – исследуются связи, возникающие между отдельными элементами и их группами. В таких случаях могут выделяться обобщающие значения, результативные или те, которые определенным образом влияют на обобщающие.
Ряды распределения и статистические таблицы
При проведении статистического анализа пользуются построением рядов распределения. Их целью является определение самых характерных признаков и присутствующих закономерностей, действующих в совокупности. Вид рядов распределения определяется тем, какой признак лежит в основе группировки. Принимая за основу качественные показатели, получают атрибутивные группировки. Делая акцент на количественном признаке, ряд называется вариационным. В свою очередь, вариационный ряд может быть ранжированным, дискретным, интервальным.
В ранжированном ряду элементы совокупности располагаются в порядке возрастания или убывания. Так легко выявить наибольшее либо наименьшее значения. В дискретном ряду присутствует признак прерывающихся изменений. Он может выглядеть двухграфной таблицей, в которой одна графа – признак, вторая – частота его встречаемости.
Если анализируемый признак претерпевает постоянные изменения, строится интервальный вариационный ряд. В таком случае в графе для количественных показателей указывается не одно значение, а интервал от и до.
Типовые примеры с решениями и выводами для студентов
К типовым задачам по статистике в программах колледжей и вузов относятся:
- Определение моды динамического ряда.
В динамическом ряду 1, 5, 6, 4, 8, 4, 3, 4, 9 найти моду. Так как число 4 встречается чаще других, оно и является модой. Легко определить моду с помощью гистограммы.
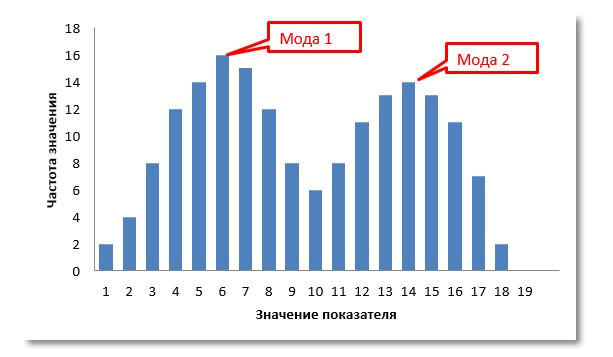
На предложенной гистограмме изображено бимодальное распределение признака.
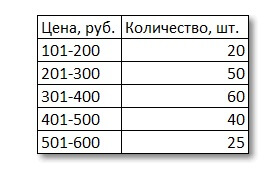
При интервальных данных задача решается чуть труднее. Допустим, даны исходные материалы:
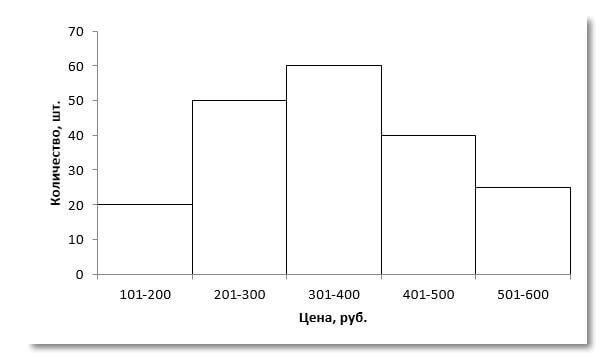
На графике модальный интервал с наибольшей частотой – 301-400 (самый высокий столбик).
Моду рассчитываем по формуле:
\(Mo=Xo+h(ƒMo-ƒMo-1)\div((ƒMo-ƒMo-1)+(ƒMo-ƒMo1)\)
где Mo-мода
Xo- начало модального интервала
h - Размер модального интервала
ƒ – частота модального интервала
ƒMo-1 – частота интервала перед модальным
ƒ Mo– частота интервала после модального
В результате расчета для данного примера Мода равна 334,3 руб
Задача № 2
Студенческой библиотекой пользуются 40 человек. Было выписано, сколько книг взял за год каждый из них. Получился результат:
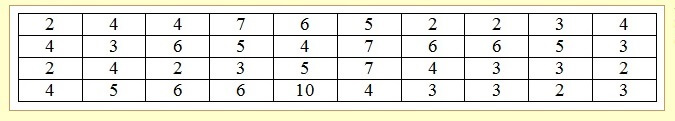
Строим ранжированный и дискретный вариационные ряды в таблице:
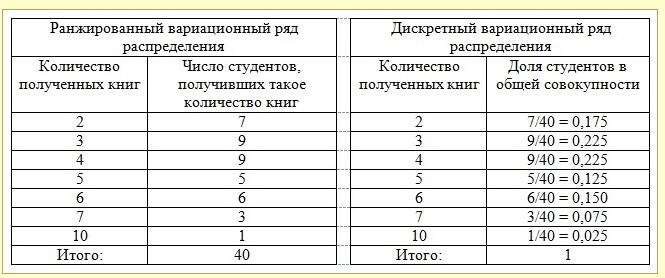
Построению таблицы предшествовало обозначение элементов ряда. Полученная совокупность содержит в себе много вариантов для анализа, как пользуются студенты библиотечным фондом.
Статистика – дисциплина, позволяющая на результатах конкретного анализа выявить наиболее проблемные либо успешные организационные моменты и провести коррекцию того или иного типового направления работы. Если нужна помощь с учебными заданиями по статистике, обращайтесь в ФениксХелп.
Пригодятся ли школьные знания в жизни
Большинство детей идут в школу с желанием: они видят в ней путь во «взрослую жизнь», надеются получить багаж знаний, приближающий к заветной профессии. Однако позже некоторые ученики начинают задумываться, а нужен ли такой широкий диапазон школьных предметов. Зачем тратить время на то, что не понадобится для будущей специальности?
Почему считают, что школьные знания не пригодится в жизни
Против предметов начальной школы обычно мало кто настроен. Конечно, умение читать, складывать и вычитать числа, излагать свои мысли на бумаге — основа коммуникабельности. В младших классах закладываются также азы иностранных языков, происходит знакомство с окружающим миром, развиваются навыки рисования, спортивные склонности. Ни родителям, ни самим ученикам изучаемые предметы не кажутся ненужными. Пессимистические взгляды появляются позднее, с введением в школьную программу специальных дисциплин.
К таким предметам относятся химия, физика, география, биология, геометрия, анатомия и другие. По мнению части учащихся, тем, кто, например, планирует стать парикмахером либо продавцом детских товаров, совершенно бесполезными будут знания по выше обозначенным предметам. С другой стороны, некоторые родители выбирают для своих детей профессии творческие либо намерены строить спортивную карьеру. Большую часть времени ребенка они посвящают тренировкам, освоению музыкальной грамоты, рисованию и т.п. Если в 4-5 классах времени хватает на все, то программы старших классов становятся настолько насыщенными, что приходится чем-то жертвовать.
Вот и возникает справедливый вопрос: почему ребенок должен «тратить время и силы не в том направлении»? Ведь программы обучения в спортивных или музыкальных школах также с возрастом обучающегося становятся сложнее, предполагают участие в конкурсах, соревнованиях, смотрах. И часто для участия в них нужно ехать в другой город, тратя «школьное время» на дорогу.
Одаренные ученики, хоть и с трудом, справляются с двойной нагрузкой. Те, у кого этого не выходит, отстают по программе и вынуждены заниматься дополнительно. А на это по прежнему нет времени и желания.
Такие рассуждения витают не только среди будущих творческих и спортивных личностей. Так же, например, может рассуждать ребенок потомственных врачей, которому некогда заморачиваться с задачами по физике. Аналогично — будущий лингвист, испытывающий трудности при изучении химии и анатомии. Примеров из жизни можно приводить много, однако следует рассмотреть и другую точку зрения.
Какие школьные предметы найдут свое применение во взрослой жизни
Каждый человек, кроме профессиональной деятельности, вынужден решать массу бытовых вопросов. Обеспечивая самому себе условия для нормальной жизнедеятельности, отлично, когда он ориентируется в вопросах:
- как выбрать полезные продукты питания;
- как построить свой рабочий день с минимальным вредом для здоровья;
- какие материалы использовать для строительства или ремонта жилья;
- как не довести до аварийной ситуации собственный транспорт;
- как приготовить еду, соблюдая правила безопасности;
- как правильно организовать досуг своим близким с учетом их интересов (например, уход за цветами, разведение домашних животных и т.п.);
- как сориентироваться в маршрутах предстоящих путешествий и т.д.
Перечень вопросов бесконечен. И какое нервное напряжение испытывает потом взрослый человек, если не может разобраться, казалось бы, в элементарных вещах.

Вот и получается, что знания, закладка которых происходит в школе, вовсе не лишние.
Где в жизни пригодится физика
Разделы школьной программы по физике охватывают нашу жизнь всесторонне. Если человеку никогда не придется двигать мебель, просчитывая самый короткий путь, он каждый день пользуется электроприборами и обязан знать, что такое электрический ток. Кроме этого, вокруг нас постоянно присутствуют небезопасные электромагнитные поля, часто — рентгеновское излучение, а иногда появляется опасность радиационного характера. Современный человек, не ориентирующийся в сути этих физических явлений, не сможет вовремя принять решение и помочь предотвратить беду.
Нельзя назвать бесполезными знания по оптике или электростатическим процессам. А с особенностями перехода вещества из одного состояния в другое каждый из нас сталкивается ежедневно, например, при кипячении воды либо замораживании продуктов.
Где в жизни пригодится математика
Относятся ли к необходимым знаниям по математике? Существует множество профессий, владея которым человек не сталкивается с математическими закономерностями. Но это только на первый взгляд. И дело даже не в магазинах, в которых надо платить по чеку. Кто, проводя ремонты, не вспоминал шуточное изложение теоремы Пифагора: «Пифагоровы штаны во все стороны равны»? Как врач прочитает кардиограмму, не имея знаний по геометрии? Как айтишник станет профессионалом, не зная характеристик операционных систем, а художник создаст трехмерное полотно? Химика, создающего искусственные продукты питания, ткани или стройматериалы, не знающего математику, также сложно себе представить.
Вот и получается, что прав Хуго Штейнхаус, который говорил: «Между духом и материей посредничает математика».
Какие еще предметы будут не лишними
Четко обозначить «лишние» предметы в школьной программе вряд ли у кого получится. Для многих на первое место «по ненужности» выходят физкультура, черчение, ОБЖ, обществознание и др. Некоторые предлагают вывести предметы в отдельный блок и преподавать тем, для кого они перспективны. Однако стоит рассмотреть их детально.
- Тому, кому в детстве не была привита любовь к физкультуре, трудно во взрослой жизни настроится на спорт. А, испытывая дефицит движения, люди с сидячим образом жизни подвержены риску развития заболеваний сердца, позвоночника, глаз, органов пищеварения.
- Фундаментом любого изделия, конструкции или сооружения является чертеж. Он существовал даже тогда, когда наука «черчение» еще отсутствовала. Надо ли говорить, что азы черчения применяются при графическом изображении окружающих предметов? Кроме того, оно развивает пространственное мышление и воображение, включая в этот процесс оба полушария головного мозга. Человек лучше ориентируется в пространстве, интуитивно читает обозначения, обращает внимание на знаки и символы.
- Основы безопасности жизнедеятельности — реально полезный и содержательный предмет. В ходе его изучения часто обращается внимание на жизненные ситуации, к которым у всех уже выработалось привыкание, однако от этого они не стали безопаснее.
- Отдельный разговор — об обществознании. Мнение о ненужности предмета ошибочно, поскольку член социума должен ориентироваться в закономерностях его развития. Овладеть знаниями по обществоведению — значит научиться применять постулаты философии, политологии, социологии на практике. Это насущно не только для будущих социологов. Экономически и социально перспективное общество должны строить сообща все его члены. И это не идет вразрез с личными профессиональными предпочтениями.
Какие знания нужно давать в школе
Научные и практические педагогические кадры современного общества много работают над созданием и корректировкой учебных программ. Их цель — сделать обучение максимально полезным и интересным, сформировать у учащихся интерес к учебе. Появление различных методик — яркое тому подтверждение. При этом основы в подходах к созданию оптимального формата преподавания остаются постоянными:
- полученные знания должны стать фундаментом для формирования всесторонне развитой личности;
- помочь обнаружить природные задатки и наклонности учащегося;
- подготовить прочную основу для получения будущей профессии.
Подробнее разобраться в программах школьного преподавания и их целесообразности помогут на ФениксХелп — здесь можно получить помощь как в написании теоретических работ, так и в организации практической деятельности.
Почему студенческие годы - лучшее время в жизни
Есть в жизни периоды, которые запоминаются на всю жизнь. К ним хочется возвращаться снова и снова. Студенческие годы — то самое время. Этот жизненный этап всегда полон позитива, ярких интересных моментов, беззаботного времяпровождения.
Правда ли, что студенческие годы лучшее время в жизни
Поступая на обучение в ВУЗ или техникум, абитуриент становится студентом. По сравнению со школой, он попадает в среду самостоятельности, туда, где нужно самому выбирать себе друзей и отвечать за принятые решения. Особенно ярко это испытывают на себе те, кто поселяется в общежитии или снимает в аренду жилье, отдельное от своей семьи. И в этом много плюсов!
Возможность научиться решать бытовые вопросы и договариваться с соседями
Первые возникающие проблемы – быт, со всеми его плюсами и минусами. Своевременно пополнить запас продуктов, приготовить еду, приобрести средства бытовой химии и гигиены, следить за порядком и исправностью электроприборов – вот далеко не полный перечень дел, за которые раньше большинство повзрослевших мальчиков и девочек не отвечало. Среди студентов такие вопросы решаются достаточно легко. Круг обязанностей делится поровну — каждый отвечает за свое.
Совместная подготовка учебных заданий
Конечно, главным для студента занятием является учеба. Лекции, семинары, практические работы, коллоквиумы, зачеты, экзамены. Учебная круговерть некоторых пугает. Однако в молодые годы всегда находится масса решений, казалось бы, неразрешимых проблем. Даже если обстоятельства сложились так, что какой-то материал упущен, конспект можно позаимствовать у друга. Если что-то недопонял на занятии, всегда найдется друг, который сможет объяснить простыми словами.
Участие в мероприятиях и конкурсах, веселый досуг
Студенчество – пора не только учебы, но и активных общественных мероприятий, включая спорт, танцы, вечера поэзии или музыки. Их инициаторами могут являться как ответственные за это сотрудники деканатов, так и культурно-массовый сектор студенческого самоуправления.
Где, если не на студенческих мероприятиях, проявить талант, которому было столько времени посвящено в школьные годы. Многочисленные спортивные турниры внутривузовского и межвузовского характера, смотры-конкурсы КВН, бальных танцев, завораживающей бардовской песни. И это не говоря о конкурсах стенгазет, юморинах, дискотеках. Студент всегда найдет время на занятия по интересам.
Особый разговор о тех, кто приехал учиться в большой город из отдаленных регионов. На все выходные дни у них расписаны экскурсии, посещения мест культуры и музыки, выставок. Данная ниша предложений сегодня настолько разнообразна, что увлечься можно не только знакомыми направлениями, но и познать новые для себя интересы.

Возможность обнаружить в себе новые таланты
Многие именно в студенческие годы открывают для себя увлечение, которое остается любимым занятием (хобби) на всю жизнь. Так, отправляясь в студенческие походы, человек на долгие годы влюбляется в туризм, а то и альпинизм.
Участвуя в смотрах-конкурсах поэзии, некоторые обнаруживают таланты в написании стихов. Для других открывается мир изобразительного искусства или фотографии. Когда еще можно беззаботно стоять на набережной и писать пейзажи? Или фотографировать проходящих мимо людей, получая удовольствие от искренних эмоций? Таким образом можно и денег заработать. Главное, чтобы это было талантливо и душевно.
Важное:
Много чего нового можно узнать и сделать в эти годы. В качестве знаменитого примера можно привести Марка Цукерберга, который в студенческий период сумел придумать то, что впоследствии стало «Фейсбуком» и сделало его богатейшим человеком планеты.
Возможность развивать коммуникативные навыки
Стать ярким, коммуникабельным человеком. Например, в студотряде многие проявляют неординарный организаторский талант, а те, кто от природы был стеснительным, становятся заводилой и душой компании.
Можно получить опыт общения и с коллегами из зарубежных стран. Сегодня довольно много программ по обмену в рамках специальности. Гораздо проще попасть в число счастливчиков, если у вуза имеются соответствующие договоренности. Если нет, можно самостоятельно найти варианты. В качестве примера можно рассмотреть программы AIESEC или WORK and TRAVEL USA.
Возможность проявить себя и зарекомендовать претендентом на серьезное будущее открывается перед теми, кто участвует в серьезных студенческих форумах, например, «Ладога», «Таврида», «Балтийский Артек», «Территория смыслов на Клязьме» и другие. Здесь не только царит доброжелательная атмосфера, но и завязываются многообещающие знакомства, формируются компании по интересам.
Почему студенческие годы лучше, чем школьные
Для многих яркими воспоминаниями являются школьные годы. Именно друзья, с которыми сидел за одной партой, часто идут рядом по жизни. Доказано, что браки бывших одноклассников оказываются наиболее крепкими. Залогом длительности отношений выступают совместные воспоминания и привязанность.
Однако, в отличие от студенческих лет, школьник редко бывает самостоятельным в выборе интереса. Чаще родители, по-своему оценивая важность того или иного занятия, прививают ребенку интерес. Вот и получается, что прирожденный хоккеист занимается игрой на скрипке, а будущий писатель танцует народные танцы.

Студенческие годы – самый подходящий период почувствовать и проявить себя, сделать выбор в пользу своих истинных интересов.
Что сделать, чтобы так было на самом деле
Для этого придется немного постараться. Ведь можно, просидев за учебниками, не заметить, как срок обучения пролетел. Для того чтобы студенческие годы стали яркими и запоминающимися, нужно:
- Быть активным, участвовать в массовых мероприятиях. При этом можно проявить собственный талант, а можно помочь товарищу, организовав группу поддержки. Результат: интересно проведенное время, масса положительных эмоций и новые друзья.
- Стараться как можно теснее вживаться в «студенческий социум». Когда человек в центре событий, он просто не сможет остаться незамеченным. А, значит, жизнь будет выразительной и разносторонней.
- Нужно учиться всему, что предлагает жизнь (в рамках разумного, конечно). Чем больше проб будет сделано, тем проще будет определить, что именно интересно. При этом не стоит забывать о собственной индивидуальности.
- Стараться получать удовольствие от каждого события. Ведь не только любимые занятия могут приносить позитив. Вполне возможно, откроются новые таланты, которые позднее пригодятся в жизни.
- Грамотно распределять свое время. Тогда его хватит и на учебу, и на личные интересы. Ведь основное занятие студента – учеба, а сделать ее увлекательной – задача номер два.
- Лао Цзы сказал: «Не суетись! Всему свое время». Не стоит бросаться «во все тяжкие» с момента поступления на учебу. Гораздо полезнее присмотреться, отмечая именно те события, которые близки характеру.
Чем можно заняться во время учебы, чтобы запомнить навсегда
В некоторых вузах программа занятий на каникулах довольно широко охватывает различные отрасли. Например, собираются группы единомышленников по сплавлению по рекам на катамаранах, байдарке, рафте, восхождению в горы или прыжкам с парашютом. Студенты исторических факультетов находят интерес в археологических экспедициях и раскопках.
Интересны также мероприятия по сбору песенного либо поэтического фольклора, знакомству с народными традициями различных народов. Такие события надолго запоминаются и несут позитивный заряд. Знакомясь с рукотворными промыслами, девушки на всю жизнь могут полюбить вышивку, вязание, а парни – например, гончарное дело.
Если улыбнется судьба, можно попробовать принять участие в кинопробах или сняться в массовках кинофильма.
Куда можно записаться, в каких мероприятиях принять участие
- спортивные состязания;
- конкурсы красоты;
- тематические вечера типа «Мой друг – гитара»;
- выставки работ изобразительного искусства;
- презентации книг, фильмов;
- КВН;
- студенческие юморины;
- конкурсы современного либо народного танца.
Проводите студенческие годы весело, а с учебой всегда поможет ФениксХелп.
Решение задач на расчет концентрации растворов по химии
Смесь, состоящая из частиц растворителя, растворяемого вещества и продуктов их взаимодействия, называется раствором. Это гомогенные структуры однородной консистенции, состоящие из двух либо нескольких компонентов. Решение задач на растворы – определение их концентрации, степени растворимости веществ, условий протекания растворообразующих процессов.
Задачи на растворы по химии
Чистое вещество либо смесь нескольких компонентов, попадая в растворитель, могут проявлять свойства:
- хорошей растворимости;
- малой растворимости;
- быть нерастворимыми.
При растворении в воде образуются многочисленные атомно-молекулярные связи. Их количество зависит от коэффициента растворимости – химической величины, которая рассчитывается путем деления массы растворяемого вещества на массу растворителя.
Кроме этого, в задачах могут присутствовать массовая доля вещества, растворенного в соответствующем растворителе.
Как решать задачи с процентными растворами
Растворы с выраженной концентрацией активного (растворенного) вещества носят название процентных. В задачах по химии ставятся цели определить содержание массы растворенного вещества, массы образовавшегося либо первоначального раствора, процентного содержания вещества до или после растворения.
Растворы, о которых идет речь в задачах по химии, обладают общими свойствами:
- они однородны;
- смешивание компонентов происходит за малый отрезок времени, как и изменение их концентрации;
- в результате смешивания двух (или более) растворов с различной концентрацией, происходит не только увеличение общей массы и объема раствора, но и усреднение процентного содержания растворенного вещества.
Поэтому существуют общие принципы их решения. Так, увеличение концентрации происходит в результате упаривания (испарения растворителя), а уменьшение – разбавления. В результате смешения может наблюдаться как увеличение, так и уменьшение, в зависимости от конкретных условий задачи.
В любом случае характеристики начального и конечного продуктов будут различаться, поэтому важно, данные в условии сведения не перепутать. Для этого применяется их нумерация.
Чтобы грамотно составить алгоритм решения, часто бывает полезно использовать уравнение химической реакции относительно активного вещества либо кислоты.
Концентрация растворов и способы ее выражения

На бытовом уровне понятие концентрации раствора выражается в отношении массы растворенного вещества к массе раствора, выраженном в процентах. Однако правомерно более широкое определение, охватывающее различные способы выражения концентрации.
Концентрация раствора – количественный показатель состава активного вещества в растворе, выраженное в определенных единицах и заключенное в единице массы или объема. Выражается в долях, процентах, массовых долях, молярности, мольных долях, титрах. Из них чаще применяются молярность и мольная доля.
1. О массовой доле (\(\omega\)) идет речь в задачах, когда можно составить соотношение масс растворенного компонента и всего раствора. Для ее выражения существует формула:
\(\omega=M_{в-ва}\div M_{р-ра}\)
Выражается она в процентах либо долевых частях единицы.
2. Молярность (по-другому – молярная концентрация) или \(С\) показывает сколько молей растворяемого компонента содержится в литре раствора. Ее формула имеет вид:
\(С=n\div V\)
где \(n\) – это растворенное вещество в молях. Исходя из его значения, раствор может быть одномолярным (содержит 1 моль в 1 литре), децимолярным (0,1 моля в 1 л), сантимолярным (0,01 моль) и т.д.
3. Концентрация моляльная (обозначается \(С_х\)) – моляльность – показатель количества (n) молей растворенного компонента в 1 кг растворителя (\(M_{р-ля}\)).
\(C_x=n\div M_{р-ля}\)
4. Для определения содержания (в граммах) вещества в 1 л раствора применяется понятие «титр» (\(Т\)).
\(T=M_{в-ва}\div V_{р-ра}\)
5. Под растворимостью (\(S\)) понимают максимальную массу растворяемого вещества, способного раствориться в 100 г растворителя:
\(S=(M_{в-ва}\div M_{р-ля})\times100 {}\)
6. Коэффициент растворимости (\(K_s\)) – показатель, который определяется отношением массы вещества к массе растворителя при условии получения насыщенного раствора при обозначенной температуре:
\(K_s=M_{в-ва}\div M_{р-ля}\)
Решение задач на упаривание растворов
Выпаривание раствора происходит в результате испарения воды, что ведет за собой уменьшение общего объема и массы. В то же время масса растворенного вещества остается без изменений. Существуют случаи, когда, кроме растворителя, испаряется растворенное вещество, если оно обладает повышенной летучестью.
Пример. Водный раствор аммиака
Рассмотрим пример решения задачи на упаривание.
Условие: В наличии 800 г раствора с 15%-ной концентрацией определенного вещества. Нужно увеличить его массовую долю на 5%. Сколько г воды должно испариться?
Этапы решения:
- Какова масса вещества в первичном растворе?
\(M_в=\omega_в\times M_р=0,15×800=120\)г, где \(M_в\) - масса вещества, \(M_р\) - масса раствора
Найденное значение останется постоянным, поскольку при выпаривании изменения массы растворенного вещества не происходит. Значит M’=120г
2. \(M_р=M_в\div\omega_в= 120÷0.2=600\)г
3. Теперь можно найти массу испаренной воды:
\(M{исп\;в}=M_р-M’=800-600=200\)г
Решение задач на разбавление растворов
В результате процесса разбавления масса того вещества, которое растворено, не меняется в отличие от массы всего раствора и растворителя.
Задача
Масса имеющегося раствора NaCl 200г, его концентрация – 15%. К раствору добавлено 40г воды. Определить массовую долю NaCl в конце реакции.
Решение
1. Определение массы раствора в конце процесса:
\(M’=M_{р-ра}+M_{добH2O}=240\)г
2. Определение массы NaCl в начале процесса:
\(M_{NaCl}=(\omega_{NaCl}\times M_р)\div100\%=15\%\times200г\div100\%=30 {}\)г
В конечном растворе \(M’_ {NaCl}=M_{NaCl}\)
3. Определение массовой доли NaCl в конце процесса:
\(\omega’_{NaCl}=M_{NaCl}\div M’_р\times100\%=12,5\%\)
Решение задач на концентрирование растворов
Повышение концентрации происходит при добавлении вещества в раствор. При этом конечная масса растворенного вещества равна сумме первоначального содержимого и того, который добавлен.
Задача. Имеется 180 г раствора с 8%-ной концентрацией соли (формула NaCl). В этот раствор всыпали еще 20 г поваренной соли. Какая массовая доля NaCl получилась в конце реакции?

Решение
1. Определение окончательной массы раствора:
\(M’_р=M_р+M_{доб}=200\)г
2. Определение конечной массы NaCl:
M’=M+Mдоб
Следовательно, нужно найти \(M\) – массу в начале процесса.
\(M=(\omega_{NaCl}\times M_р)÷100%=14,4\)г
Тогда \(M’=14,4г+20г=34,4\)г
3. Определение массовой доли NaCl в конечном продукте:
\(\omega’=M’_{NaCl}\div M’_р\times100\%=17,2%\)
Решение задач на смешение растворов
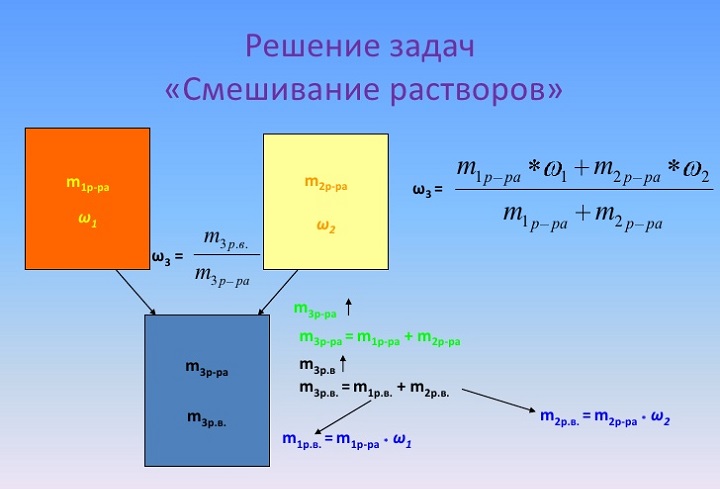
Смешение растворов с различной концентрацией растворенного вещества происходит с соблюдением «конверта Пирсона». Это – диагональная модель, при которой нельзя складывать массовые доли, а можно – лишь массы растворенных компонентов и растворов.
Задача
Дано два раствора с массами \(M\) и \(M_1\). Массовые доли растворенного вещества обозначим соответственно \(ω\) и \(ω_1\). В конечном продукте аналогичная величина – \(ω_3\). Необходимо приготовить третий раствор с отличной от имеющихся концентраций.
Решение
1. Определение общей массы растворенного вещества:
\(M_1\omega_1+M_2\omega_2=\omega_3(M_1+M_2)\)
2. Математические действия:
\(M_1(\omega_1-\omega_3)=M_2=(\omega_3-\omega_2)\)
\(M_1\div M_2=(\omega_3-\omega_2)\div(\omega_1-\omega_3)\)
Следовательно, согласно этому математическому выражению, и нужно взять соотношение растворов.
Задачи на определение процентной концентрации раствора
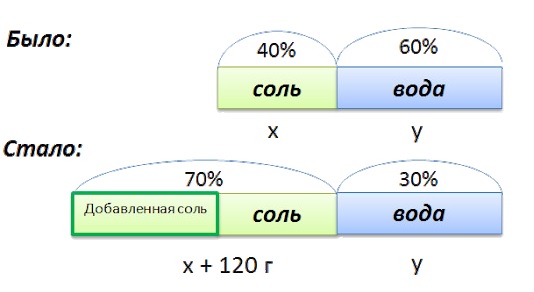
Задача 1
Какая процентная концентрация раствора \(KNO_3\), если нормальная равна \(0,2\) моль/л. Плотность равна \(1\) г/мл.
Решение:
1. Определение массы раствора объемом \(1000\) мл:
\(M=\rho\times V=1\times1000=1000\)г
2. Составление и решение следующей пропорции:
\(20,0\)г \(KNO_3\) - \(1000\) г раствора
\(Х_г\) - \(100\) г раствора
\(Х=2,02\) г или \(ω=2,02%\)
Задача 2
Нужно приготовить \(300\) г 25%-ного раствора соли, имея 60%-ный и 10%-ный. Сколько нужно взять таких компонентов (m1 и m2)?
Для решения применим правило Креста:
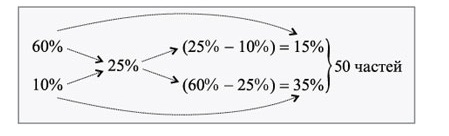
1. Определение веса одной из 50-ти частей образуемого раствора:
\(300\div5=6\)
2. Определение массы каждой части \(m_1\) и \(m_2\):
\(m_1=6\times15=90\)
\(m_2=6\times35=210\)
Задача 3
Используя 250г 45%-ного раствора соли, нужно понизить его концентрацию до 10%. Сколько воды необходимо использовать?
Концентрация соли в воде, используемой в качестве добавки, равна 0.
По методу креста образуется 45 частей раствора:
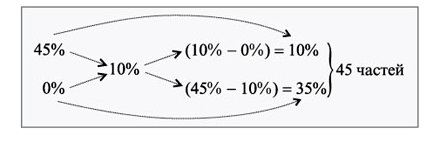
Решение
1. Масса одной части первичного раствора равна: \(250\div10=25\)г
2. Определение массы воды, что необходима: \(25\times35=875\)г
С целью проверки можно выполнить следующие действия:
1. Определение массы конечного продукта-раствора:
\(875+25=1125г\)
2. Для исходного раствора действует пропорция:
В 250г 40%-ного р-ра содержится Хг соли
в 100 г – 45г
Отсюда Х=112,5 г соли
3. Определение конечной концентрации раствора:
1125 г раствора – 112,5 соли
100г – Х
Х=10г или 10%
Следовательно, нужно взять 875 г воды.
Решать задачи на растворы – интересное занятие! Знание основных закономерностей будет полезно с теоретической и практической точек зрения. Однако бывают случаи, когда нужно быстро сдать контрольную либо перепроверить собственные решения. Тогда можно обратиться на сайт ФениксХелп.
