Современная теория строения атома
Сегодня даже дети дошкольного возраста знают, что все вокруг состоит из молекул и атомов. А вот что это такое и из чего они, в свою очередь, состоят — знает далеко не каждый взрослый. В этой статье просто и доступно, поделимся современными знаниями о мельчайших частицах.
Что такое атом — история открытия
Итак, все окружающие нас объекты и мы сами состоим из крошечных частиц, которые называются атомами. В их состав входят еще меньшие частицы: протоны, нейтроны и электроны. Современное строение атома наука открыла сравнительно недавно, до этого его долго считали неделимой частицей.
Мысль о том, что все вокруг состоит из мельчайших, невидимых глазу частиц возникла в Древней Греции и Древней Индии еще до нашей эры. Древнегреческий философ Демокрит был материалистом. Именно он первым ввел в обиход понятие атома (с греческого — atomos — неделимый). Демокрит считал, что невидимые частицы вечны, их бесчисленное множество, они постоянно двигаются, обладают весом, размером и формой.
Последующее развитие теория атомизма получила в Средние века и Новое время в работах французского физика Пьера Гассенди (1592—1655 гг.) и английского ученого Роберта Бойля (1627-1691 гг.).
Развитием атомистической теории и превращением ее в атомно-молекулярное учение занимались также Ломоносов, Лавуазье, Дальтон.
Долгое время атом считали элементарной, т.е. неделимой частицей. Но в 1897 году Джозеф Дж. Томсон открыл первую субатомную частицу — электрон. Это открытие имело огромное значение. Ученый впервые предложил определенную структуру строения, считавшейся ранее неделимой частицы, которая получила название «пудинг с изюмом». Согласно этой модели атом — это положительно заряженная сфера, внутри которой находятся отрицательно заряженные электроны.
Но теорию Томсона опроверг Эрнест Резерфорд. В 1917 году британским физиком было совершено открытие протона — положительно заряженной элементарной частицы. Открыв протон, Резерфорд предположил и наличие нейтронов — нейтрально заряженных частиц в атоме. Позже их существование экспериментально подтвердил Джеймс Чэдвик. Основываясь на своем открытии, Резерфорд предложил свое описание атомной модели: положительно заряженное ядро и окружающие его электроны.
В 1913 году датчанин Нильс Бор предложил свой вариант строения атома, получивший название «планетарной модели». Согласно теории Бора, электроны находятся на определенном расстоянии от атомного ядра и вращаются по специальным орбитам (по аналогии с планетами, вращающимися вокруг Солнца).
В начале XX века планетарную модель заменила волновая модель, принятая научным сообществом во всем мире.
Современные представления о строении атома были бы невозможны без открытия элементарных частиц и явления радиоактивности. Огромный вклад в науку, помимо вышеназванных ученых, внесли Эрвин Шредингер, Макс Планк, Вольфганг Паули.
Атомная структура — современные знания
На чем базируется, из скольки главных частиц состоит
Основу современных представлений теории атомизма составляют следующие положения:
- Атом состоит из ядра и окружающей его электронной оболочки.
- Электронная оболочка представляет собой движущиеся вокруг ядра электроны.
- Ядро всегда положительно заряжено — оно состоит из протонов, обозначающихся символом — p и нейтронов — n. Заряд ядра всегда равен сумме протонов в нем.
- Атом электронейтрален, так как число отрицательных частиц — электронов (е–) равняется числу положительных частиц — протонов (p+).
- Его электронейтральность может нарушаться, при условии, что он отдает или присоединяет электроны, при этом он становится положительно или отрицательно заряженным ионом соответственно.
- Электроны располагаются вокруг ядра в трехмерном пространстве. Они находятся в специальных областях, которые называют орбиталями. Каждая из этих областей характеризуется формой, размером и ориентацией внутри атома, каждой из орбиталей присваивается буквенно-цифровое обозначение.
Свойства, масса и размер
Большую часть атома составляет полупустое пространство, заполненное электронами. Ядро — это самая тяжелая (99,97% от массы атома) и одновременно самая маленькая его часть. В ядре как раз и сосредоточена практически вся масса атома. Ее измеряют в а.е.м. — атомных единицах массы. Атомная единица массы равна массе 1/12 части атома углерода, свободно покоящегося и находящегося в основном состоянии. В химии используют «моль» для измерения атомной массы. 1 моль — это количество вещества, содержащее число атомов, которое равно числу Авогадро.
Массовое число — это сумма нейтронов и протонов в ядре атома.
Размеры атомов крайне малы. Самым маленьким по размеру считается атом Гелия, его радиус составляет 32 пикометра. Атом цезия является самым большим, его радиус равен 225 пикометров. Пико = \(10^{-12}\). А радиус ядра в 10 000 раз меньше радиуса атома.
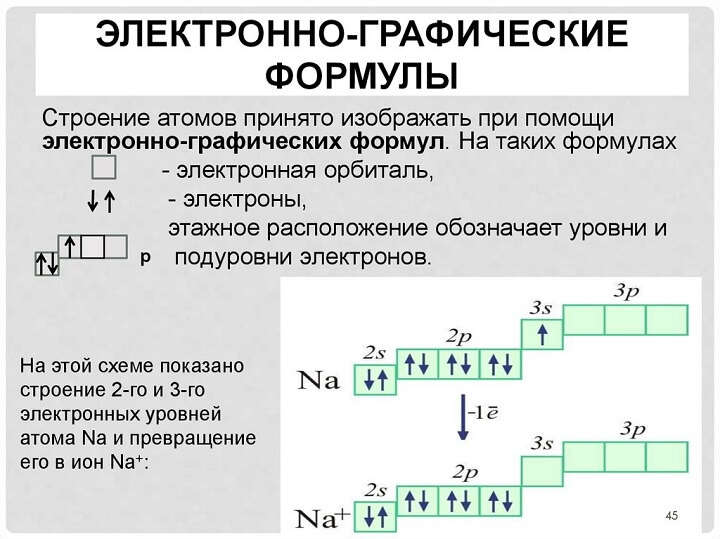
Электронно-графическая формула
Периодическая система и строение атома, какая взаимосвязь
В таблице Менделеева указывается относительная атомная масса химических элементов.
Количество протонов в ядре соответствует порядковому номеру химического элемента в известной таблице Менделеева. Заряд ядра — это главная характеристика атома, которая влияет на распределение вещества в таблице Менделеева.
Количество нейтронов в таблице не указывается, их можно рассчитать, вычтя из массы атома порядковый номер химического вещества (число его протонов).
Почему ядро не распадается
Науке известно 4 основных вида взаимодействия между телами и частицами:
- слабое;
- сильное;
- электромагнитное;
- гравитационное.
Внутри атома, в его ядре, между протонами и нейтронами существует сильное взаимодействие, которое не позволяет ядру с легкостью распадаться. В середине XX века человечество обнаружило, что при расщеплении ядер происходит высвобождение огромной энергии, что послужило толчком для развития атомной промышленности и ядерного оружия.
Атомистическая теория — не самая сложная тема, которая есть в физике и химии. Если столкнулись с заданиями посложнее и не понимаете, с чего начать, ищите помощи у специалистов Феникс.Хелп!
Понравилась статья?
Подпишитесь на наш блог и получайте наши статьи первым!
Или подписывайтесь на нас в соцсетях:
Заметили ошибку? Выделите текст и нажмите одновременно клавиши «Ctrl» и «Enter»
Нашли ошибку?
Текст с ошибкой:
Расскажите, что не так


Бесплатно отвечаем на ваши вопросы. Задайте свой вопрос и получите ответ от профессионального преподавателя. Выберите лучший ответ.
Вопросы могут задавать только авторизованные пользователи. Войти